| 导 读
2019年9月21日, 上海科技大学姜标课题组、阴倩倩博士、杨小宝博士在Journal ofMedicinal Chemistry (IF: 6.259)杂志上,发表题为“Discovery of SIAIS178 as an effective BCR-ABL degrader by recruiting von Hippel–Lindau (VHL) E3 Ubiquitin Ligase”的研究论文,研究人员发现了一个致癌融合蛋白BCR-ABL降解剂,通过诱导BCR-ABL和von Hippel-Lindau(VHL)E3泛素连接酶之间的适当相互作用,导致BCR-ABL蛋白有效降解,在靶向蛋白水解的嵌合PROTAC对BCR-ABL驱动的CML细胞系K562细胞的生长抑制作用实验中,IC50值达到24 ± 2.9nM, 在体外实现BCR-ABL白血病细胞的显著生长抑制。
| 内 容
慢性粒细胞白血病(CML)是一种骨髓增生性疾病,其特征在于费城(Ph+)染色体及其嵌合致癌产物BCR-ABL的存在。BCR-ABL表现出组成性激活的ABL酪氨酸激酶活性,可刺激下游信号传导途径,导致CML细胞不受控制地增殖。
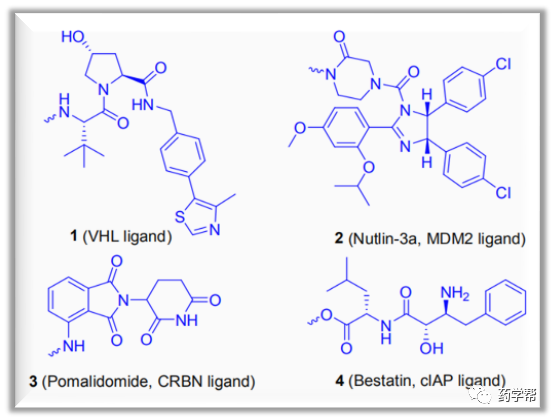
图1. 报道的小分子E3配体 (图片来源于JMC期刊)
靶向蛋白水解的嵌合(PROTAC)技术作为发现几种小分子E3泛素连接酶配体后消除翻译后蛋白功能的药理策略而受到关注,因此还发现了针对BCR-ABL的有效降解剂,且更紧密的空间邻近性以促进VHL E3连接酶和目标蛋白之间的有利蛋白质-蛋白质相互作用(PPI)。
图2.报道的基于达沙替尼的靶向BCR-ABL的PROTAC分子(图片来源于JMC期刊)
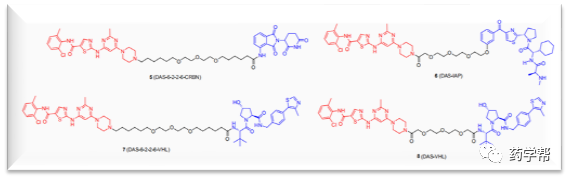
图2. 报道的基于达沙替尼的靶向BCR-ABL的PROTAC分子(图片来源于JMC期刊)
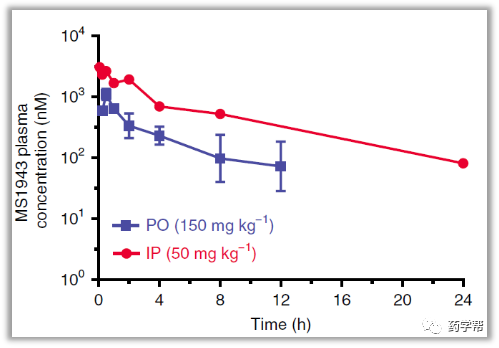
上海科技大学姜标课题组、阴倩倩博士、杨小宝博士考虑到接头的长度和柔韧性会显着影响PROTAC的降解效果,研究团队推测接头的长度和组成可能未得到充分研究,优化的接头可诱导BCR-ABL靶标与VHL E3连接酶之间的良好相互作用,因此导致BCR-ABL降解。研究团队描述了通过连接ABL激酶抑制剂达沙替尼dasatinib和VHL E3泛素连接酶配体1(VHL1)来设计,合成和评估新型BCR-ABL降解物的方法。在K562细胞中评估实验发现对其BCR-ABL降解活性的效力构效关系表明PEG(-O-CH2-CH2-O-)的氧对PROTAC的降解有不利影响,所以最佳接头长度应包含5〜10个碳原子,以促进这些PROTAC达到BCR-ABL降解的最大功效。经过研究团队的努力发现了SIAIS178(19),可在体外和体内有效降解BCR-ABL蛋白,在体外实现CML细胞的显着生长停滞,在体内通过单剂量静脉内(IV)或腹膜内(IP)注射SIAIS178(19)进行的药代动力学研究,腹膜内给药后的药代动力学数据显示出良好的药代动力学特性,且针对K562异种移植肿瘤诱导产生实质性的肿瘤消退效果。机理研究表明,BCR-ABL和VHL连接酶之间19诱导的正确的三元复合物的形成可能是其降解能力增强的主要驱动力。
这项工作意义重大,尽管靶向BCR-ABL的酪氨酸激酶抑制剂TKI已彻底改变了CML治疗,但临床耐药性和长期药物管理仍然是一个问题。SIAIS178(19)能够诱导了一些临床相关的赋予耐药性的突变的降解,并且在短期治疗后去除药物后,与BCR-ABL激酶抑制剂相比,对CML细胞生长和活力的抑制作用更加持久和持久。
总结:上海科技大学姜标课题组为了进一步延迟BCR-ABL激酶抑制剂抗性突变的出现并解决终身药物管理的问题,开发具有不同机制的新策略。通过广泛优化连接子连接达沙替尼dasatinib和VHL1连接配体,介绍了新型BCR-ABL降解剂的设计,合成和评估。在这项研究中,证实了该接头对于PROTAC降解目标蛋白至关重要。而且,研究团队的努力已经产生了有效的BCR-ABL降解子SIAIS178(19),具有良好的选择性,在体外对BCR-ABL白血病细胞具有显着的生长抑制作用,在体内针对K562异种移植肿瘤诱导产生实质性的肿瘤消退效果。BCR-ABL和VHL连接酶之间和SIAIS178(19)诱导的适当相互作用可能是其增强降解能力的主要驱动力。此外,与ABL激酶抑制剂相比,短期治疗后药物去除后,SIAIS178(19)还诱导了几种临床相关的赋予耐药性的突变的降解,并发挥了更持久的细胞应答。数据表明,通过招募VHL E3泛素连接酶,SIAIS178(19)是最有效,最有效的BCR-ABL降解剂。它值得对BCR-ABL 白血病的治疗进行广泛的研究,这项新技术可能为克服BCR-ABL激酶抑制剂的耐药性提供新的可行策略。
附录:化合物合成路线
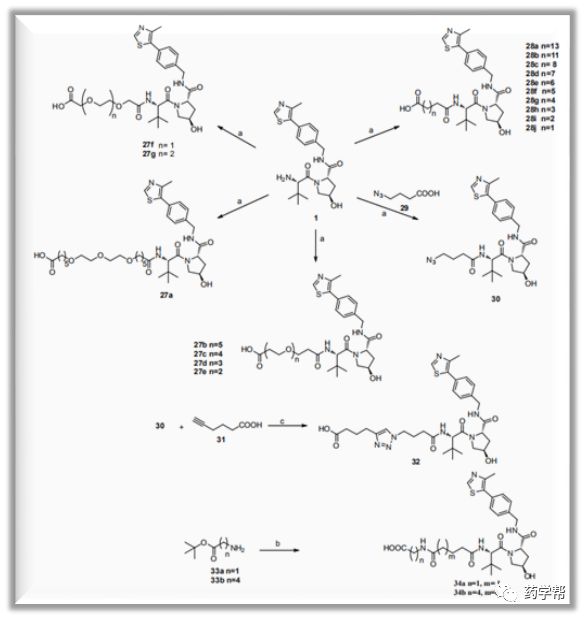
图3. VHL配体1共轭接头的合成(图片来源于JMC期刊)(a) NMM, HOAt, EDCI,DMF/DCM, 0 - 25 °C, 12h; (b) i: 28c, or 28i HOAT, EDCI, NMM, DMF, 25 °C, 12h; ii: TFA, DCM, 25 °C, 12h; (c) CuSO4, Sodium ascorbate, DMF/t-BuOH/H2O, 25°C, 12h.
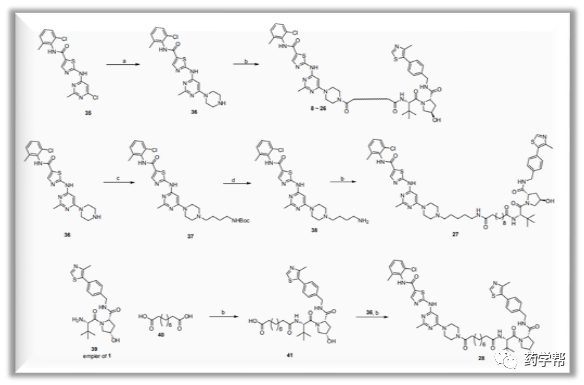
图4. 致癌融合蛋白BCR-ABL靶向蛋白水解的嵌合合成(图片来源于JMC期刊)(a) Piperazine, DIPEA,n-BuOH, 110 °C, 16h; (b) 27a~g, or 28a~j, HOAt, EDCI, NMM, DMF, 25 °C, 12h; (c)NMP, DIPEA, 100 °C, 3h; (d) TFA, DCM, rt., 2h.
✔姜彪教授简介

姜标,有机化学教授,博士(图片来源于上海科技大学官网)
个人简介
姜标于1962年11月出生于中国福建省,他获得兰州大学的化学学士、硕士学位,并获得了兰州大学和上海有机化学研究所(SIOC)的联合博士学位。在SIOC进行了两年的博士后研究后,他于1990年成为SIOC的助理教授,然后于1992年获得早期晋升为副教授的资格。他于1994年成为正式教授。在SIOC的职业生涯中,他担任过副主任,研究所所长。2012年,他被任命为上海科技大学上海高级免疫化学研究所所长。他在SIAIS的研究专注于转化医学,包括使用聚焦化合物库,抗体药物结合物(ADC)和基因疗法进行药物前导发现。
教育经历
1988年,博士学位,化学,兰州大学和上海有机化学研究所(SIOC)联合学位
1986年,兰州大学化学硕士
1983年,兰州大学化学学士
工作经历
2012年至今,上海科技大学上海高级免疫化学研究所(SIAIS)教授
2009年至今,中国科学院上海高级研究所教授
1994年至今,SIOC教授
1992-1994年,美国杜邦大学药物化学客座科学家
1992-1994年,上海国际商学院副教授
1990-1992年,上海国际商学院助理教授
1988-1990,博士后,SIOC
社会兼职
联合国环境规划署化学技术选择委员会联合主席
联合国环境规划署技术和经济评估小组成员
上海国际制药有限公司创始人兼董事长
上海辛尼卡有限公司创始人兼董事长