| 导 读
2019年8月13日, 中山大学药学院尹课题胜组在Journal of Medicinal Chemistry (IF:6.259) 杂志上,发表题为“Germacrane Sesquiterpenoids as a New Typeof Anticardiac FibrosisAgents Targeting Transforming Growth Factor βType I Receptor (TβRI)”的研究论文,研究人员发现了吉马烷倍半萜作为一种新型抗心纤维化药物,靶向转化生长因子βI型受体(TβRI),该药物可在微摩尔水平上抑制转化生长因子β1(TGFβ1)刺激的心脏成纤维细胞中纤连蛋白(FN),α-平滑肌肌动蛋白(β-SMA)和胶原蛋白的表达,作用机理研究表明该药物能够抑制TGFβ1/small mother against decapentaplegic (Smad)靶向TGFβI型受体的信号通路,IC50达到(14.9±1.6 nM),能够改善主动脉收缩(AAC)大鼠腹部的心肌纤维化和心脏功能。
| 内 容
心脏纤维化是各种心血管疾病的常见病理结果,例如高血压心脏病和心肌梗塞,其特征是心肌组织中细胞外基质(ECM)蛋白的过度合成和病理积累,在心室重构中起关键影响,导致心肌僵硬并导致舒张性心力衰竭。大量证据表明,心脏纤维化改变可能是可逆的,这表明合理设计的抗纤维化疗法在控制心血管疾病方面可能具有不可估量的价值。但是,一般来说,目前尚无针对纤维化疾病的有效疗法,这在很大程度上是因为纤维化的根本基础难以捉摸。
近年来,对促进成纤维细胞转化的分子途径进行了深入研究,发现了涉及多种激素和细胞因子的复杂信号网络,其中发现the small mother against decapentaplegic(Smad)依赖型TGFβ信号传导被认为是成肌纤维细胞转化和心脏纤维化的主要调节因子。在正常心脏中,一旦激活就会磷酸化TGFβII型受体(TβRII),进而磷酸化TGFβI型受体(TβRI,也称为ALK5)。磷酸化的TβRI可以进一步磷酸化Smad2 / 3,从而产生磷酸化的Smad2 / 3,然后与Smad4形成复合物,转移到细胞核中,最终激活ECM的下游基因转录。因此,在心脏纤维化疾病中,阻断TGFβ/ Smad信号传导的药物被认为是有研究价值的疗法。
中山大学药学院尹胜课题组基于先前的研究,发现云南马兜铃的粗提物对心肌纤维化具有治疗作用。随后经化学研究分析分离出一组倍半萜类化合物.这些倍半萜类化合物对TGFβ1刺激具有一定的抗心肌纤维化作用。心脏成纤维细胞及其机制研究表明,它们对TGFβ/ Smad信号通路具有抑制作用。在该研究中,基于该植物主要成分马兜铃内酯的结构修饰,构建了包含30种化合物倍半萜类化合物库。
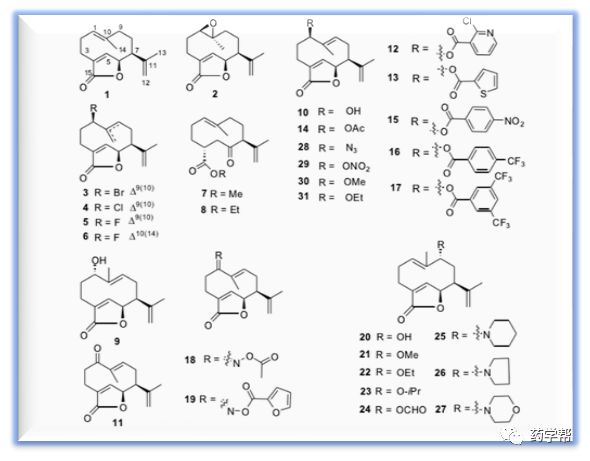
图1.吉马烷文库中化合物(1-31)的结构(图片来源于JMC)
该文库的系统筛选鉴定出的化合物11,是一种据有前途的抗心纤维化药物,具有明确的机制和体内显着的疗效。在化合物1-31的初步筛选心脏纤维化生物标志物FN实验中,化合物11被确定为活性最高的化合物,在10μM时将FN含量降低至26.1±4.1%。还评估了化合物11的细胞毒性,当浓度为25μM时,对心脏成纤维细胞的活力没有明显的抑制作用;化合物11可以剂量依赖性地降低FN,γ-SMA和胶原I、 III在2.5、5和10μM时的蛋白水平。因此,这些生物标志物的mRNA水平也被下调。在TGFβ1的刺激下,细胞核中Smad2和Smad3的含量增加,而10μM化合物11的处理下显着降低了细胞核中的mad2和Smad3含量,并相应地增加了在细胞质中的含量。这些结果表明化合物11抑制了TGFβ信号通路中Smad2 / 3的磷酸化和核易位;化合物11还表现出对TβRI激酶的有效抑制作用,IC50值为14.9±1.6 nM。这些结果表明化合物11是心脏成纤维细胞中潜在的抗纤维化剂。
这项研究有深远的意义,TGFβ/ Smad信号抑制剂FT01115和TβRI抑制剂SM1616和GW78838817先前已被证明在动物模型中是有效的抗心纤维化剂。但是,相关的不良心脏作用阻碍了它们进一步进入临床研究。因此,新型的具有明确作用机制和较少副作用的TGFβ/ Smad信号抑制剂的发现十分重要。
总结:以前有报道称云南马兜铃中的倍半萜类化合物对TGFβ1刺激的心脏成纤维细胞具有一定的抗心肌纤维化作用,但这些化合物的潜在靶标,构效关系和体内功效尚不清楚。中山大学药学院尹胜课题组基于该植物主要成分马兜铃内酯的结构修饰,构建了包含30种倍半萜类化合物库。该文库的系统筛选出化合物11被鉴定为一种有前途的抗心纤维化剂,具有明确的机制和体内显着的功效。化合物11能以微摩尔水平抑制TGFβ1刺激的心脏成纤维细胞中ECM(FN和胶原蛋白)和γ-SMA的积累,并以5 mg / kg剂量改善主动脉收缩AAC大鼠的心肌纤维化和心脏功能。机理研究表明,化合物11通过抑制TβRI来阻断TGFβ/ Smad信号通路(IC50=14.9±1.6 nM)。构效关系研究表明,不饱和γ-内酯环和C1的氧化对活性很重要。值得注意的是,与SB431542相比,化合物11具有更好的酶促活性,但细胞活性较弱,这表明在未来的修饰中仍需要努力提高化合物11的细胞膜通透性。这些发现可能为将来针对心脏纤维化及相关疾病的药物开发提供启示
附录:化合物合成路线
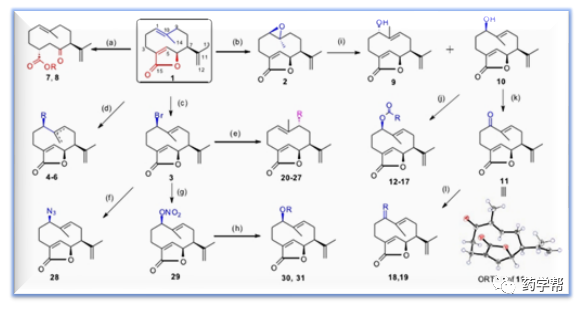
Scheme1. 吉马烷衍生物的合成(图片来源于JMC期刊)
(a)NaOMe, CH3OH, rt, 30 min, 85% for 7; NaOEt, EtOH, rt,1 h, 40% for 8; (b) m-CPBA, CH2Cl2, rt, 30 min,92%; (c) N-bromosuccinimide (NBS), CH2Cl2, rt, 30 min, 82%;(d) N-fluorobenzenesulfonimid (NFSI), NaH, CH2Cl2, 0-25 ℃, 3 h, 35% for 5 and 32% for 6; N-chlorosuccinimide(NCS), CH2Cl2, rt, 1 h, 56% for 4; (e)dimethylsulfoxide (DMSO)/H2O = 100:1 (v/v), 60 ℃, 14% for 20; MeOH, 50 ℃, 1 h, 75%for 21; EtOH, 60℃, 2 h, 71% for 22; NaH, IPA, 0-50℃, 3 h, 32% for23; HCOOH, N, N-dimethylformamide (DMF), 80℃, 1 h, 15% for 24;piperidine/pyrrolidine/morpholine, DMF, 50℃, 1 h, 15% for 25, 54% for 26,46% for 27; (f) NaN3, DMF, 60℃, 1 h, 14%; (g) AgNO3, EtOH, rt,10 min, 40%; (h) MeOH, 40℃, 30 min, 68% for 30; EtOH, 50℃, 1 h, 52% for 31;(i) 1% HCl in MeOH (m/v), 50℃, 3 h, 12% for 9 and 68% for 10; (j)2-chloronicotinyl/2-thiophenecarbonyl/acetyl/4-nitrobenzoyl/2-trifluoromethylbenzoyl/3,5-bis(trifluoromethyl)benzoyl chlorides, Pyr, 80℃, overnight, 52% for12, 62% for 13, 93% for 14, 42% for 15, 50% for 16, 47% for 17; (k) IBX, DMSO, 60 ℃, 2h, 92%; (l) NH2OH·HCl,NaOAc, MeOH, rt, 30 min, then acetyl/2-furoyl chlorides, Et3N, CH2Cl2, rt, 1 h, 43% for 18 and 37% for19.
✔尹胜教授简介

尹胜(图片来源于中山大学药学院官网)
简历:尹胜,中山大学药学院教授博士生导师国家优青、广东省杰青、广东省“青年拔尖人才。
2003年毕业于复旦大学化学系化学专业,获学士学位,同年保送至中国科学院上海药物研究所硕博连读,专业为天然药物化学。2008年博士毕业,获中科院院长特别奖(获40万启动经费),中科院优秀博士论文提名奖等。2008年10月至2010年6月在澳大利亚Eskitis研究所从事以高通量筛选为导向的海洋天然产物研究,导师为Eskitis研究所所长Ron. Quinn院士。2010年10月作为中山大学“百人计划”副教授、博导引进,2014年1月晋升为教授。迄今从三十余种高等植物及海洋生物中分离鉴定约500多个化合物,其中200多个为新化合物,新颖碳骨架类型10种,其中3个化合物被天然产物权威评论性杂志 Natural Product Reports选为热点化合物(Hot off the press),部分化合物具有重要的生物活性,已开发成为先导化合物。在JMC、Organic Letters, Journal of Natural Products等SCI杂志上发表论文70多篇,其中通讯及第一作者SCI科研论文60篇(平均IF>3.0, 有10篇为top15%期刊平均IF>5.0)。研究领域为以活性筛选为导向从天然产物中提取、分离、鉴定结构新颖的活性小分子化合物,并进行结构修饰和相关的药理活性研究
研究方向:
天然药物化学、天然有机化学
教育经历:
2014/01——至今 中山大学药学院,教授,博士生导师
2010/11——2013/12 中山大学药学院,“百人计划”副教授,博士生导师
2008/06——2010/06 澳大利亚Eskitis研究所,博士后研究员
2008/06——2010/10 中国科学院上海药物研究所,助理研究员
2003/09——2008/07 中国科学院上海药物研究所,药物化学,博士
1999/09——2003/07 复旦大学,化学系,学士
社会/学术任职:
中国化学会会员;广东省现代中药工程技术研究中心海洋药物化学实验室主任;国内核心期刊《天然产物研究与开发》青年编委;国际期刊Organic letters、 Steroids、 Bioorganic & Medicinalchemistry常邀审稿人