| 导 读
2019年7月3日,北京大学药学院张亮仁和刘振明课题组在J. Med. Chem.杂志上,发表题为“Multistage Screening Reveals 3-substituted Indolin-2-one Derivatives as Novel and Isoform Selective c-Jun N-terminal kinase 3 (JNK3) Inhibitors: Implications to Drug Discovery for Potential Treatment of Neurodegenerative Diseases”的论文,课题组发现了一个强的JNK3抑制剂J30-8,它是作为第一个被证实具有体外神经保护活性和体内抗AD功效的亚型选择性JNK3抑制剂,J30-8可通过抑制皮质和海马中JNK、APP和tau蛋白的磷酸化作用,显著减少弥漫性和纤维状Aβ斑块。药代动力学研究表明,J30-8具有较高的有效血浆暴露和一定量的脑内分布,与药效学结果一致。有望成为阿尔茨海默病治疗的候选药。本文来源于药学帮,未经授权严禁转载。
| 内 容
阿尔茨海默病(AD)是世界上最具挑战性的疾病之一,缺乏有效的临床治疗。以前的研究表明c-Jun N末端激酶3(JNK3)是治疗AD的一个有吸引力的靶点。
北京大学张亮仁和刘振明课题组近日报道了一系列3-取代吲哚-2-酮衍生物作为第一个亚型选择性JNK3抑制剂。在这项研究中,进行了基于结构的虚拟筛选, J30-8表现强的IC50值(40nM),具有2500倍以上的异构体选择性和显著的Kinome宽选择性。进一步研究表明,1μM的J30-8在体外表现出神经保护活性,通过减少斑块负荷和抑制JNK、aβ前体蛋白和tau蛋白的磷酸化来减轻体内空间记忆损伤。J30-8作为已证实的亚型选择性JNK3抑制剂,可作为进一步研究AD的JNK3的候选物,也可作为开发JNK3抑制剂用于神经退行性疾病的潜在治疗药物。
北京大学张亮仁和刘振明课题组近日报道了一系列3-取代吲哚-2-酮衍生物作为第一个亚型选择性JNK3抑制剂。在这项研究中,进行了基于结构的虚拟筛选, J30-8表现强的IC50值(40nM),具有2500倍以上的异构体选择性和显著的Kinome宽选择性。进一步研究表明,1μM的J30-8在体外表现出神经保护活性,通过减少斑块负荷和抑制JNK、aβ前体蛋白和tau蛋白的磷酸化来减轻体内空间记忆损伤。J30-8作为已证实的亚型选择性JNK3抑制剂,可作为进一步研究AD的JNK3的候选物,也可作为开发JNK3抑制剂用于神经退行性疾病的潜在治疗药物。本文来源于药学帮,未经授权严禁转载。
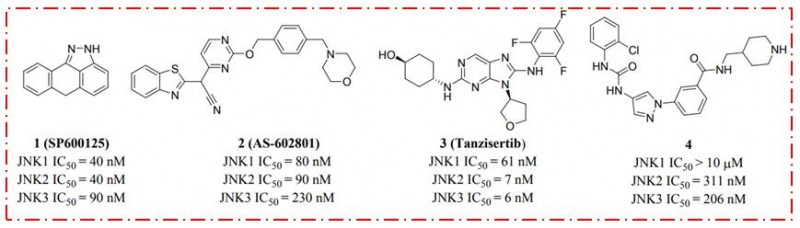
图1. 文献报道的JNKs抑制剂(图片来源于JMC期刊)
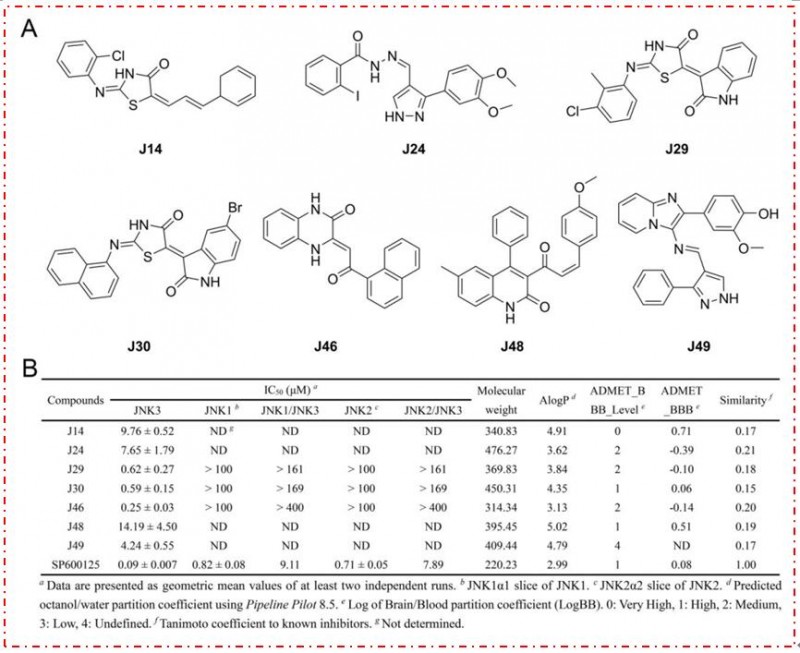
图2.(A)合成的7种JNK3抑制剂的化学结构。(B)已鉴定的JNK3抑制剂的酶活性和代表性分子特性(图片来源于JMC期刊)
研究者最终鉴定出几种新的JNK3骨架抑制剂,其中三种化合物J29、J30和J46在纳摩尔水平上显示出JNK3 活性。基于这些化合物的结构骨架的进一步优化,发现了JNK3的 IC50值为40nM的化合物J30-8,对JNK1α1和JNK2α2的异构体选择性超过2500倍,对筛选的398激酶的Kinome宽选择性优异。本文来源于药学帮,未经授权严禁转载。
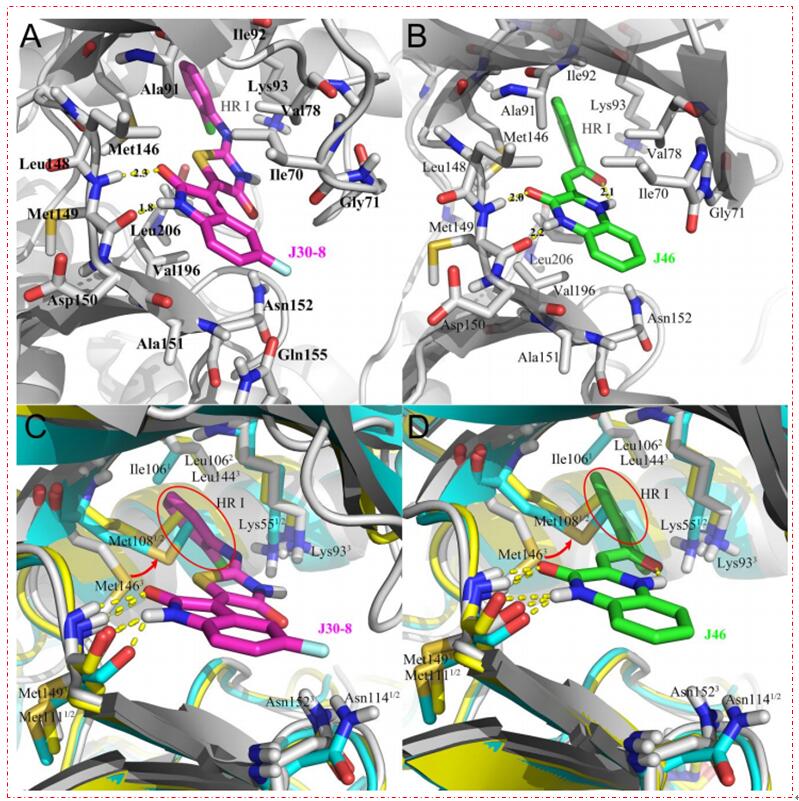
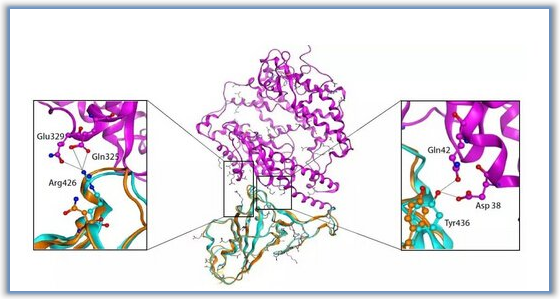
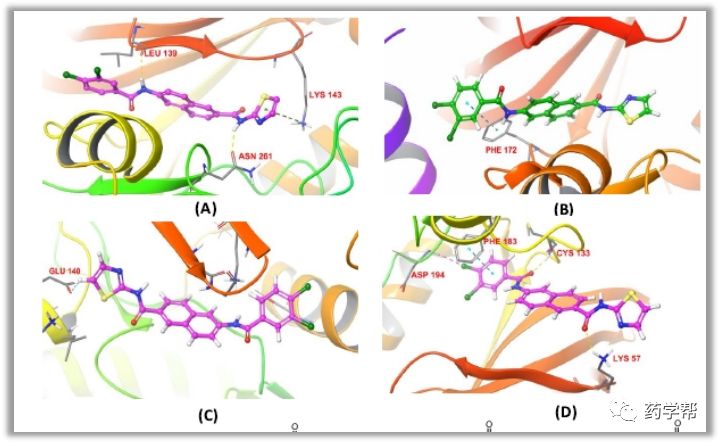
图3.化合物J30-8(A)和J46(B)的预测结合模式。JNK3(PDB ID 4whz和4w4w,灰色)、JNK1(PDB ID 3pze,浅蓝色)和JNK2(PDB ID 3e7o,黄色)晶体结构与化合物J30-8(C)和J46(D)的叠加。氢键用黄线表示。HR I=疏水区域I。pymol软件作为表现结合模式的图像。(图片来源于JMC期刊)
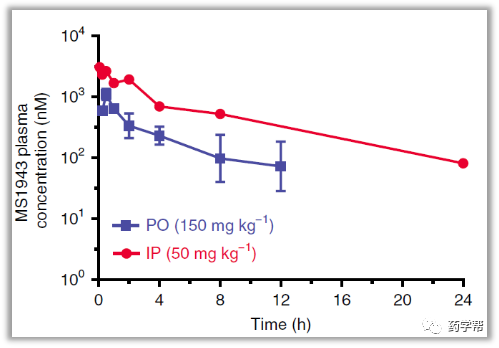
此外,化合物J30-8在体外表现出与LICL相当的神经保护活性,并显著提高了APPSWE/PS1DE9小鼠的学习和记忆能力。进一步的机制研究表明,J30-8可通过抑制皮质和海马中JNK、APP和tau蛋白的磷酸化作用,显著减少弥漫性和纤维状Aβ斑块。药代动力学脑渗透研究表明,J30-8具有较高的有效血浆暴露和一定量的脑内分布,与药效学结果一致。因此,J30-8作为第一个被证实具有体外神经保护活性和体内抗AD功效的亚型选择性JNK3抑制剂,可以作为进一步研究JNK3与AD的有用工具,也可以作为JNK3抑制剂在神经退行性疾病潜在治疗中的开发。

张亮仁教授(图片来源于北京大学官网)
个人介绍
张亮仁,1963 年出生。北京大学教授、博士生导师、北京大学药物化学系主任。兼任中国药学会药物化学专业委员会委员,Heterocycles、Drug Discov. Ther.、Molecules、《药学学报》、《中国药物化学杂志》、《中国药学(英文版)》、《中国药学杂志》等期刊的编委或顾问编委。主要从事核苷、核苷酸及寡核苷酸药物的设计合成、构效关系研究,以及以结构为基础的药物设计与合成。先后主持包括国家自然科学基金、教育部博士点基金、新药创制重大专项等在内的多项科研项目。在国内外学术杂志发表研究论文170 余篇,曾获2002 年教育部自然科学奖二等奖(第2 完成人)、 2004 年国家自然科学二等奖(第2 完成人)。
研究领域
1.核苷、核苷酸及寡核苷酸药物的设计与合成
2.以结构为基础的药物设计与合成以及构效关系研究
3.有机小分子对细胞信号传导系统的调控研究

刘振明副研究员
学习经历
1996-2000 理学学士,北京医科大学药学院药物化学专业
2000-2005 理学博士,北京大学化学与分子工程学院物理化学专业(导师:来鲁华)
工作经历
2011年-至今 副研究员,北京大学药学院本文来源于药学帮,未经授权严禁转载。
2005年-2011年 讲师,北京大学药学院
2007年-2009年 “重大新药创制”科技重大专项实施管理办公室
研究方向
1)发展新的药物设计方法,并将其应用于药物的发现过程。
2)通过设计和结构修饰生物活性分子针对特定的药物靶标寻求找到新的具有应用价值的活性先导化合物。