| 导 读
2019年7月11日,南京大学化学化工学院蒋锡群课题组、胡勇课题组、美国北卡罗来纳大学Zhen Gu课题组在Nature Communications (IF: 12.124) 杂志上,发表题为“Eradication ofunresectable liver metastasis through induction of tumour specific energydepletion”的论文,南京大学作为第一单位。研究人员发现了一种能够选择性杀死肝转移癌细胞的方法,并在基因和蛋白质水平上探讨了潜在的分子机制。
| 内 容
肝癌是一种严重的恶性肿瘤,具有高转移率,易致死等特点的重大疾病。迄今为止,外科手术是临床上处理肝癌转移最有效的方法,不幸的是,大多数肝癌转移病例被发现时已经是晚期,手术预后效果差。
弥漫性肝癌转移是以多发性转移结节为特征,患病后会快速恶化。肝脏作为一个负责高强度代谢活动的器官,本身极易受到化疗相关并发症的影响,从而缩短患者化疗后的生存期。一些新出现的治疗药物,如伊尼帕里布和尼拉帕里布,能够通过利用合成致死机制,抑制具有独特基因组特征的癌细胞。尽管在一定程度上对患者有所帮助,但若用来治疗肝癌转移效果很差。此外,它们都属于精确到分子水平的治疗,适应症较窄。因此,发展更有效的治疗方法来延长弥漫性肝癌转移患者的寿命仍是一项紧迫任务。
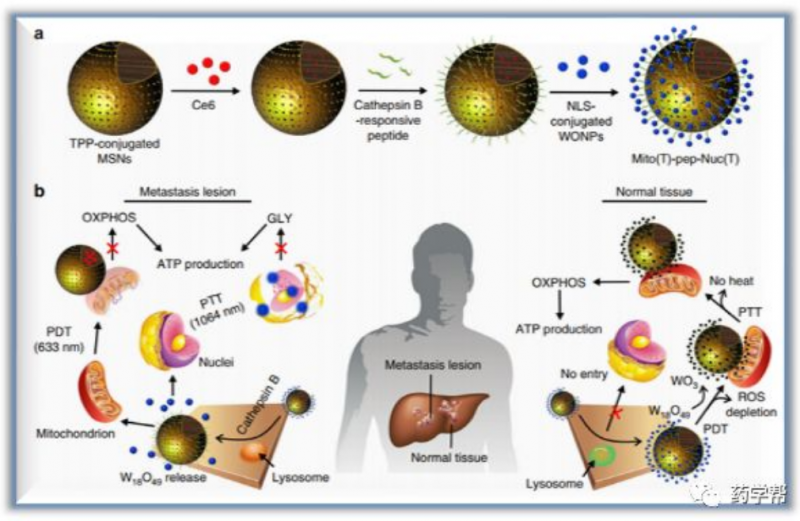
图1. Mito(T)-pep-Nuc(T)工作原理(图片来源于NatureCommunications)
近日,南京大学化学化工学院蒋锡群课题组、胡勇课题组、美国北卡罗来纳大学Zhen Gu课题组,发现了一种能够选择性地杀死肝转移癌细胞的策略。由于精确到细胞水平的靶向输送在大多数情况下对癌细胞和健康细胞都是有害的,没有选择性。因此,如何利用靶向机制的传递策略,使病变位置成为药物积聚的唯一位置至关重要。为了不影响正常细胞的同时且能够有效治疗弥漫性肝癌转移,研究人员考虑采用非主动靶向给药的替代方法,目的是通过利用肿瘤普遍存在的病理特征来限制癌细胞的作用。
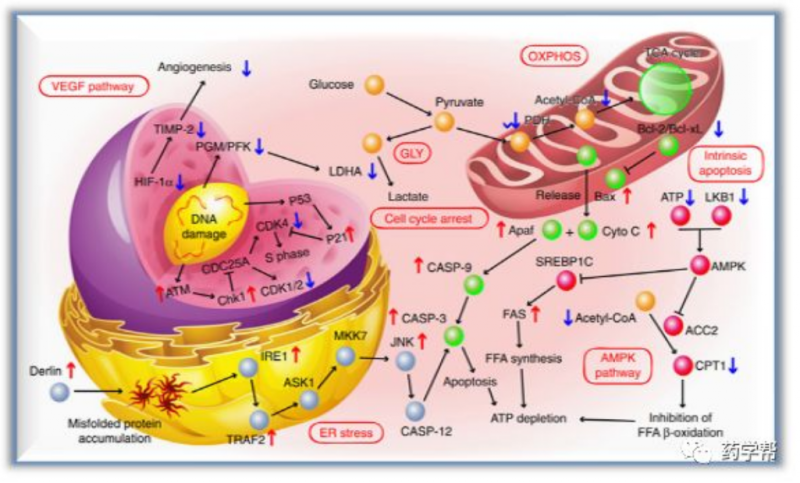
图2. Mito(T)-pep-Nuc(T)在癌细胞的治疗中可能的信号通路(图片来源于NatureCommunications)
作者合成了一种由光敏剂(Ce6)包封的介孔二氧化硅纳米粒子和W18O49纳米粒子组成的混合体系。线粒体选择性介孔二氧化硅纳米粒子和W18O49纳米粒子分别与三苯基膦(TPP)和核定位序列(NLS)功能化,从而使它们与线粒体和核进行选择性结合。在癌细胞中,Mito(T)-pep-Nuc(T)在富含组织蛋白酶B的溶酶体中破裂,释放具有不同亚细胞的Mito(T)和Nuc(T)。随后,分别应用激光照射(633nM,随后1064nM)来依次触发Ce6和WONPs介导的光动力疗法(PDT)和光热疗法(PTT)。两种细胞器都可能被破坏,共同破坏ATP供应。同时,由于组织蛋白酶B活性不足,肽连接体在肝细胞中保持完整。在633nM激光照射下,产生的单峰氧可被WONP化学计量消耗,从而将其转化为光热惰性WO3,并在1064nm激光照射下消除产生热量。因此,肝细胞可以从PDT和PTT引起的破坏中解救出来。
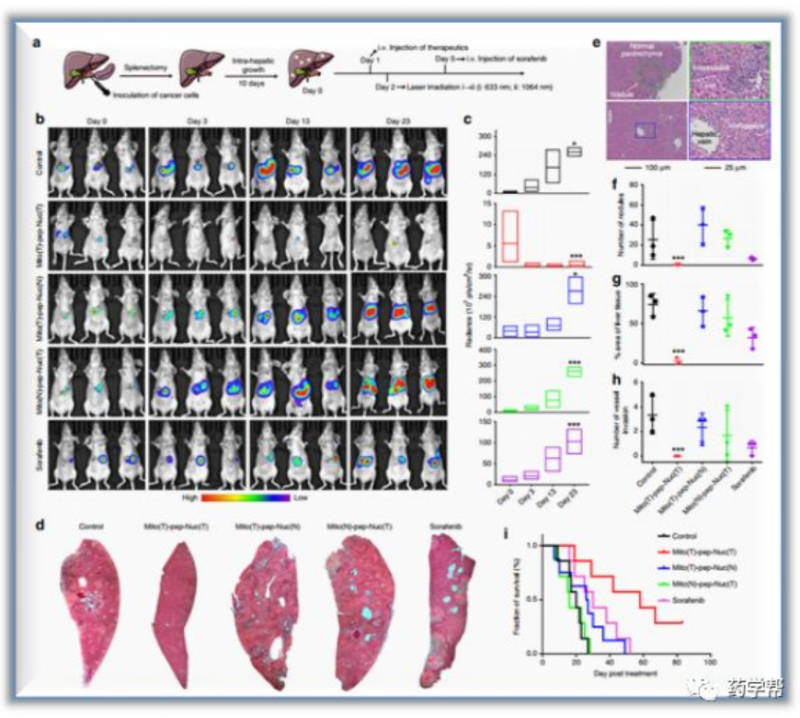
图3. 体内抗转移作用(图片来源于NatureCommunications)
在肝细胞中,通过激光照射产生的单重态氧物质被wops消耗,导致其光热加热能力丧失,使肝细胞免受激光照射引起的热损伤。相比之下,在癌细胞中,分裂的肽连接体允许wops和msns分别靶向细胞核和线粒体,从而释放药效。这会引起癌细胞能量来源被消除,从而达到选择性地杀死肝转移癌细胞的目的。作者进一步在基因和蛋白质水平上探讨了潜在的分子机制,以更好地理解治疗结果。
总结:该研究,作者充分考虑到复杂的肝脏生态位置,进行了全新靶向策略的设计。实验证明同时阻断癌细胞中gly和oxphos的活性可以有效地消除肝转移癌细胞,同时不影响正常肝细胞。基于代谢的肿瘤选择性治疗策略在该研究中被证明是通过利用能量消耗机制来克服肝转移癌细胞。研究人员考察了它们与细胞成分的相互作用及其对细胞代谢方式的影响。进一步的炎症反应验证结果,证实了该策略的有效性和兼容性。
✔蒋锡群教授简介

蒋锡群教授(图片来源于南京大学官网)
【个人简历】
蒋锡群,1983年本科毕业于南京大学化学系,1986年硕士毕业于南京大学化学系高分子材料专业,1995年被教育部选派以中日联合培养博士生身份赴日本九州大学学习,并于1998年获南京大学博士学位。1999年-2000年,在美国威斯康星大学从事博士后的研究工作。现为南京大学化学化工学院教授,博士生导师,高分子科学与工程系主任,高性能高分子材料与技术教育部重点实验室主任,高分子功能构造与结构调控教育部创新团队负责人。2006年获国家杰出青年科学基金。近5年来主持了包括国家杰出青年基金及国家自然科学基金重点项目在内的十余项国家及省部项目。其研究方向为:大分子自组装、高分子药物传输系统、高分子影像材料,高分子纳米簿膜和高分子表面等。在Nature Communications, J. Am. Chem. Soc., Angew.Chem. Int. Ed., Advance Materials, ACS Nano等学术刊物上发表论文130余篇,论文他引3300余次。获美国专利授权2项,国家发明专利授权8项。获2013年度“中国化学会高分子科学创新论文奖”。
✔胡勇教授简介
胡勇教授(图片来源于南京大学官网)
【个人简历】
1993年9月进入南京大学化学化工学院高分子系,1997年获学士学位、2002年获博士(2002)学位。2002年7月到2003年12月在南京大学物理系系进行博士后研究;2003年12月到2004年12月在新加坡国立大学-约翰霍布津斯大学联合研究院做博士后;2005年11月到2006年3月,2008年9月到2008年10月,在新加坡-麻省理工联合研究院做博士后研究;2010年7月到2011年8月,德国Duisburg-Essen大学化学系洪堡学者。2006年3月到2006年12月,南京大学材料系讲师,2006年12月起在南京大学现代工程与应用学院任讲师、副教授、教授。
主要从事生物医用高分子材料和高分子复合材料的研究,包:生物降解高分子医用材料、聚电解质纳米材料、高分子纳米药物载体以及非病毒性纳米基因载体,纳米磷酸钙骨组织工程材料。与合作者在Angew. Chem. Int. Edit.,Adv. Mater.,Biomaterials, Biomacromolecules,J. Control. Release,Chem. Comm. 等重要国际学术刊物发表论文40多篇,总引用超过1000次(其中,单篇论文引用超过100次的有3篇)。已经申请发明专利6项,获得一项关于快速止血的纳米生物材料的世界专利1项(US 60/479,096)。作为项目负责人获得多项国家自然科学基金。在高分子复合材料研究领域,主要研究特殊用途纳米涂层复合物材料及粘合剂,和企业合作开发的产品获得2010年教育部科技进步推广类二等奖(金属表面高性能纳米防护技术及产业)。获德国洪堡基金会的资助,在德国Duisburg-Essen大学进行为期一年的洪堡学者研究。Advanced Powder Technology的国际编委。